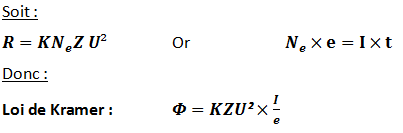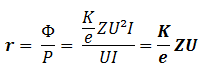Présentation
Autre nom :
- Tomodensitométrie (« tomos » = section ; « densitométrie »= mesure de densités)
- CT : computerized Tomography
- CAT Scan : computerized Axial Tomography
Technique d’imagerie par rotation qui utilise les photons X pour créer des images axiales, anatomiques et parfois fonctionnelles.
Matériel :
- Table (avec un poids limite : 250kg en général)
- Statif (tube, détecteurs, générateur) : il peut s’incliner selon les protocoles
- Console de l’opérateur (avec arrivée d’image en quasi temps réel)
Axe Z : axe tête –pied = axe du déplacement de la table
Axe X : droite gauche
Axe Y : antérieur postérieur
Unité : HOUNSFIELD : divise la partie étudiée en carré et mesure la valeur moyenne d’absorption quand ils sont traversés par un faisceau de rayons X. (technique qui date de 1968).
- 1999 : Scanner multi barrette (rotation continue + table mobile).
Définitions
- Loi d’atténuation :
- I0 : intensité de faisceaux X initial
- I : Intensité du faisceau à une distance X
- x : épaisseur traversée
- µ : coefficient d’atténuation global de toutes les matières traversées prenant compte toutes les structures de densités différentes
- Matrice : grille en deux dimensions composées de lignes et de colonnes, elle est en générale composée de 512² (pixels = unité de la matrice ; il définit la base d’une image numérique). En 3D on passe en cube (voxel = contraction de volumétrique élément, il est égal à l’épaisseur de coupe).
Principes physiques
- Principe élémentaire :
Détecteur primaire : chambre d’ionisation à la sortie du tube où on mesure I0.
Détecteur secondaire : appelé barrettes, se trouve après le patient, ou le scanner capte le nombre de photons émergeants (mesure de I).
Grâce à la rotation du tube, le scanner mesure µx sur un axe de 360°.
- Effet Compton (60 kV – 1.022 MeV)
Eléments de technologie :
- Partie informatique :
Unité centrale : reçoit les ordres de la console d’acquisition et de traitement, gère la mécanique d’acquisition, le générateur, le transfert de donné numérique, et le processeur vectoriel qui reconstruise l’image, l’archivage.
Les consoles : interface entre l’opérateur et l’unité centrale. Système d’archivage, d’acquisition, de reconstruction, le reprographie. Contrôle la partie mécanique du Scanner.
- Partie mécanique :
Générateur : fournit la haute tension (kV) qui alimente le tube. Il est souvent embarqué (dans le statif et de part et d’autre du tube – tourne en même temps que le tube). Il est caractérisé par sa puissance : . Peuvent aller de 80 jusqu’à 460 kV.
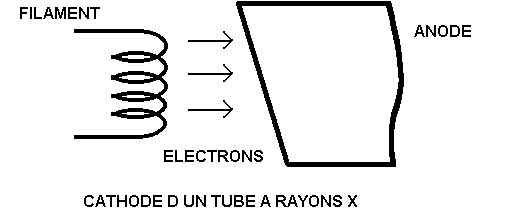
Tube à RX : grosses contraintes thermiques. Son temps de rotation est inférieur à 1 seconde (d’habitude 0.5 seconde). L’anode est faite d’un mélange de graphite, de tungstène et d’une couche de rhénium, elle tourne à 10000 tours/minutes. Le contraste (résolution et densité). Filtre en cuivre (papillon) : sert à enlever les photons de basse énergie. On essaye de rendre le faisceau monochromatique (photon tous de même énergie à car loi d’atténuation ne fonctionne qu’avec un faisceau monochromatique). A une forme de papillon (plus mince au centre que sur ses bords), homogénéise le faisceau (pour améliorer la qualité image et irradier de façon meilleur).
Collimateur primaire : diaphragme (4 lames).
FOV (Field of view = champ de vue) dans le plan XY.
Epaisseur de coupes d’acquisition (largeur d’acquisition dans l’axe Z). Ce qui permet d’irradier une partie ou la totalité des barrettes.
Limite une partie du diffusé (irradiation inutile au patient).
Le statif : se trouve tous les éléments précédemment vus. Sur le côté se trouve les boutons pour centrer le patient, se fait à l’aide de 3 lasers (sagittal, coronal, axial). Avant de faire l’acquisition on fait le 0.
La table (lit) : là où se trouve le patient. Sa vitesse de déplacement est caractérisée par le pas de l’hélice (Pitch).
Collimateur secondaire : 4 lames de tungstène qui protège les cellules du détecteur.
Grille anti diffusante : enlève de rayonnement diffusé avec changements de direction qui perturbe l’image.
Détecteurs secondaires (barrettes) : recueil de l’information I, amplifie le signal, numérise le signal (CAN). Constitué de plusieurs cellules de détection mise à coté les unes des autres (de 16 à 128 se situent dans l’axe Z), (des centaines dans l’axe x). On ne retient que les barrettes qu’on veut irradier dans l’axe Z. Il y a de 0.2 à 0.6 mm entre chaque cellule dans l’axe x. L’épaisseur d’une barrette est de 0.625 à 0.75mm. Chaque barrette à la même épaisseur (montage symétrique). Il existe aussi des montages asymétriques (4 barrettes à 1.5mm, 8 à 2.25mm et encore 4 à 1.5mm).
Détecteur gazeux (n’existe plus) : ionisation des atomes de Xénon par les photons X, des ions chargés sont collectés par une électrode, les électrons émis par cette ionisation sont captés et le courant induit est proportionnel au flux de photons X. Le flux d’électrons est amplifié (par un photomultiplicateur) puis convertit par CAN.
Rendement : capacité à capter des photons (en %) à Probabilité d’interaction faible = mauvais rendement
Rémanence : Temps au bout duquel un détecteur est de nouveau stimulable.
Détecteur solide : le faisceau X arrive sur un cristal phospholuminescant (scintillateur) qui les absorbe par effet photoélectrique qui créer des photons lumineux, qui vont taper une photodiode, qui vont créer un signal électrique. Celui-ci est proportionnel au faisceau de RX incident. Signal électrique amplifié par photomultiplicateur, puis converti par le CAN. Donc à la sortie de la barrette on a des chiffres binaires.
Rendement : capacité à capter des photons à Probabilité d’interaction fort
Rémanence : élevé
Les scanners sont bicouche pour augmenter la qualité de l’image. Il y a deux couches de détecteurs. Une couche basse intensité et une autre forte intensité.
Processeur vectoriel : relié aux cellules par des canaux de reconstruction (fibre optique). Reçoit l’information des détecteurs (barrettes) et reconstruit l’image. Stock l’image sur le disque dur et l’envoi sur la console. Capacité de stockage faible, donc on archive les images pendant 20 ans grâce à un PACS (Picture Archiving Communication System).
Reprographie : se fait sur papier glacé.
Mode d’acquisition
- Mode radio (topogramme, Scout view (surview)). Cliché radiologique numérisé obtenu par balayage du faisceau X sur l’étendue d’une région anatomique. Le tube et le détecteur ne font aucune rotation, il reste dans une position choisie. On place le tube sous la table (180°), pour éviter le diffusé. Sert à placer les coupes (programmation précise de coupe sur région d’intérêt), programmation de reconstruction d’intérêt. Permet de modulé la dose selon la densité des pixels. Les dimensions du surviews sont choisies en fonction de la région à étudier.
- Mode séquentiel : le tube fait une acquisition sur 360°, on déplace la table, re-acquisition de 360°. On a un programme automatique ou manuel. Pratique pour réduire les artéfacts cinétiques, réduction de la dose au patient. Mais il y a perte d’information entre deux coupes, information erronée si mauvais moment, temps d’acquisition plus long. Il n’est plus du tout utilisé.
- Mode dynamique : rotation continue du tube et des détecteurs sans mouvements de la table. Emission de rayons x ininterrompus et pendant une durée d’acquisition. Utilisé dans des séquences dite perfusion (AVC ischémique), injection de produit de contraste dans la zone à examiner. Le problème de ce mode c’est que c’est très irradiant pour le patient. Utilisé aussi pour un angioscanner, on passe un ROI (Région Of Interest), petite ellipse qui mesure la densité en temps réel.
- Mode hélicoïdale : rotation continue du tube et des détecteurs pendant le déplacement de la table. La rotation est constante mais c’est la vitesse de déplacement de la table qui varie. Pour relier ces deux paramètres entre eux il y a le PITCH (pas de l’hélice), rapport entre vitesse de déplacement de la table et l’épaisseur de coupe au cours d’une acquisition. Il n’y a plus de perte d’information quand l’hélice est jointive ou chevauchée.
- Coupe espacée si entre les deux parties du ressort il y a une perte d’information (P>1).
- Coupe chevauchée si hélices rapprochées (P<1).
- Coupe jointives si hélices collées (P=1).
Paramètres d’acquisition
Détermine la qualité du faisceau X et la manière dont il interagit avec le patient. Définit la qualité et la quantité de donnée brut du volume exploré.
Les constantes
- kV : tension aux bornes du générateur, différence de potentiel entre anode et cathode, donne la pénétration du faisceau. Détermine le contraste.
3 choix : 90 (surview et enfant) – 120 (presque toutes les acquisitions, région à fort contraste naturel) – 140 (structure dure à traverser, crane par exemple).
- mA : intensité du flux d’électrons
- s : temps de rotation (0.4 – 2).
- Taille du champ d’acquisition (mm):
FOV : Field of View (champ de vue). Diamètre du champ d’acquisition dans le plan XY.
25 – 35 – 50cm. Supérieur à la taille de la région anatomique à étudier.
Epaisseur des coupes d’acquisition : Ouverture de de l’axe du collimateur primaire dans l’axe Z.
- Nombre de coupes : pour le mode séquentiel.
- Longueur d’exploration : pour le mode hélicoïdal.
- Incrément (ou incrémentation) : pour le mode séquentiel (distance séparant deux milieux de coupes successives en mm).
- PITCH : pour le mode hélicoïdal :

P < 1 : coupes chevauchées (serrées) : belle qualité image car on recueil un maximum d’information, belle reconstruction (MPR – Multi Planar Reconstruction). Très irradiant.
P = 1 : coupes jointives : pas de perte d’information, belle qualité image, belle reconstruction, temps d’acquisition plus court et moins irradiant que pour P <1.
P > 1 : coupes disjointives, ouvertes : mauvaise qualité image, perte d’informations, moins de signal (mauvais rapport signal sur bruit). Interpolation informatique : calcul informatique par le processeur vectoriel pour créer l’image. Moins irradiant et plus rapide.
Paramètres de reconstruction
- RFOV : Diamètre du champ de reconstruction dans le plan XY. Changement possible, plus grand ou plus petit du FOV d’acquisition.
- Matrice : 3 choix (356² – 512² – 1024²), nombre de pixels par surface. Voxel : projection d’un volume élémentaire du patient. Plus la matrice est grande, plus il y a de pixels, plus la reconstruction sera lente.
- Epaisseur de coupe de reconstruction : Choisi après l’acquisition et en fonction de ce que l’on veut voir, détail ou contraste (résolution spatiale ou résolution en densité). Ne peut pas être à l’inférieur à l’épaisseur des barrettes, ni supérieure à la taille de l’épaisseur de coupe d’acquisition.
- Incrémentation : Il s’agit de l’incrémentation dans un volume d’acquisition, c’est-à-dire de l’espace entre 2 milieux de coupes successives. Cela ne s’applique donc que pour une acquisition hélicoïdale.
- Les filtres de reconstruction : 3 familles de filtres : les filtres mou (met en évidence le contraste entre 2 structure de densité proche) – standard (compromis entre les deux) -dur (résolution spatiale). C’est un algorithme mathématique permettant de mettre en évidence le détail ou le contraste ou un compromis entre les 2. Suivant les filtres ce ne sont pas les mêmes électrons qui passent, les filtres durs induisent du bruit.
Formation de l’image
La matrice
La matrice est une grille ; c’est le support à partir duquel l’image est reconstruite ; l’image est ainsi décomposée en « petits carrés élémentaire ». Elle est choisie en fonction des choix des constructeurs mais est en général égale à 512 ². Si le manipulateur a le choix de la taille de la matrice, il faut savoir que plus elle est grande (avec un nombre de pixels élevés) plus la définition de l’image (différent de la qualité image) sera meilleure. Et plus la matrice sera grande plus la reconstruction de l’image sera lente. L’image dans tous les cas ne doit pas ressembler à un carré et doit toujours être l’exact reflet de l’anatomie du patient.
Le Pixel
Le pixel est ‘unité élémentaire de la matrice. Chaque pixel a une tonalité de gris. La taille du pixel est calculée suivant la formule suivante :
![]()
La juxtaposition de ces pixels forme l’image. C’est la formule binaire dans les pixels qui définit les niveaux de gris.
Le Voxel
Un Voxel est la projection d’un volume élémentaire de patient. C’est la représentation virtuelle des mesures effectuées dans un volume élémentaire à l’intérieur du patient. La profondeur d’un voxel correspond à l’épaisseur de coupe de reconstruction.
À l’acquisition de l’image
Toujours grâce à la loi d’atténuation, on peut connaître l’atténuation du faisceau dans une ligne du patient, mais µ est la somme des coefficients d’atténuation des différents points de la ligne. Lors d’une acquisition, le tube et les détecteurs tournent autour du patient, chaque point est donc exploré suivant différents angles, donc différents profils d’atténuation. Les profils d’atténuation (de projection) est l’ensemble des signaux électriques fournit par les détecteurs au cours d’une rotation du tube. Sur 360° il y a 1000 angles de mesure.
À la reconstruction de l’image
Toutes ces projections sont échantillonnées et numérisées par le CAN, ce qui nous donne les données brutes de l’image. Ensuite ces projections sont rétro projetées sur une matrice de reconstruction. A partir des valeurs d’atténuation mesurées par chaque détecteur, le calculateur calcule la densité de chaque pixel de la matrice.
Le principe : si on a connaissance de la somme des chiffres d’une matrice selon tous les axes, il est alors possible de déduire tous les chiffres contenus dans cette matrice.
Calcul de la densité de chaque pixel dans la matrice :
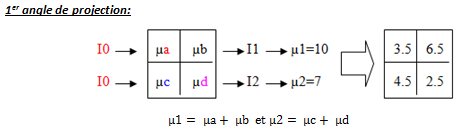
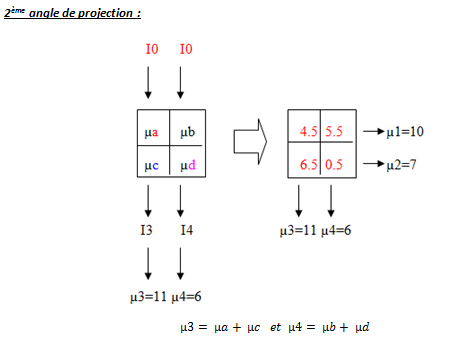
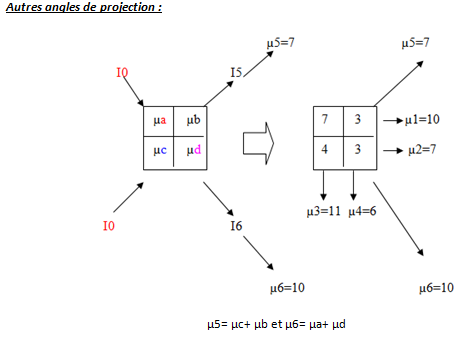
A savoir que plus il y de projections réalisées est plus le calcul des µ est précis.
Explication : I0 sont les rayons X incidents, IX sont les rayons sortants, et sont donc mesurés. Les µ sont calculés grâce aux I et à la relation d’atténuation.
Le calcul de la tonalité de gris :
Le calcul est effectué suivant la loi d’atténuation. Chaque gris traduit les µ des organes traversés. Une densité faible atténue peu le faisceau de rayons X et donne un pixel noir (hypodensité). Une densité forte atténue beaucoup le faisceau de rayons X et donne un pixel blanc (hyperdensité).
Le problème est que l’on ne peut pas voir tous les niveaux de gris produits par le scanner donc il y a une perte d’informations, en effet l’image scanner peut avoir 4096 niveaux de gris différents, le moniteur en affiche 256 et l’œil humain ne peut en distinguer que de 8 à 64.
La solution est donc de privilégier certains gris en fonction de la région étudiée et de l’indication de l’examen. D’où l’utilisation d’une échelle de gris.
L’échelle de gris ou échelle de Hounsfield :
Il s’agit d’une échelle arbitraire de gris dont les unités vont de +1000 UH (Unité Hounsfield) à -1000 UH.
+1000 UH correspond à de fortes densités et est l’unité de l’os compact et est blanc (hyperdense)
0 UH correspond des densités moyennes et est l’unité Hounsfield de l’eau.
-1000 UH correspond à des faibles densités et est l’unité Hounsfield de l’air et est noir (hypodense)
La formule mathématique reliant les UH aux valeurs de densité µ est la suivante :
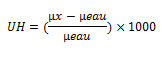
µeau est le coefficient d’atténuation linéique global de l’eau.
µx est le coefficient d’atténuation linéique global du tissu étudié.
UH calculée à la base pour 120 kV :
µair = 0 cm-1 U.H = -1000 (noir)
µeau = 0.19cm-1 U.H = 0 (gris)
µos = 0.38cm-1 U.H =+1000 (blanc) µx
Quand on augmente les kV, µeau diminue donc la valeur des U.H augmente.
Le fenêtrage (paramètre de reconstruction) :
La fenêtre est la plage des densités étudiées. Elle est caractérisée par son niveau et sa largeur.
Le niveau (level) est le centre des densités moyennes (UH) de la région à étudier « luminosité ».
La largeur (window) est l’ouverture de la plage d’exploration « contraste ».
On choisit le niveau centré sur les densités moyennes de la région à étudier
On choisit la largeur en fonction de la région étudiée:
- large pour étudier sur une même image des structures de densités éloignées sur l’échelle de Hounsfield (ex : os, poumons)
- étroite ou serrée pour étudier des structures dont les densités sont voisines (ex : abdomen, médiastin)
Pour choisir on prend : N c’est plus ou moins la largeur divisé par deux.
Exemples de fenêtrage :
- Thorax (parenchyme) N=-600 / L=1600
- Thorax (médiastin) : N=50 L=350
- Abdomen : N=50 L=350
- Os : N=400 L=2000
- Cerveau (fosse postérieure) : N=40 L=80 Cerveau (sus tentoriel) : N=50 L=150
Exemple pour thorax :
- N = -600
- L = 1600
L/2 = 800
N +/- 1600/2
Fenêtrage (niveau de gris entre = gamme de gris) :
- – 600 (N) – 800 (L/2) = – 1400
- – 600 (N) + 800 (L/2) = 200
Il faut adapter le fenêtrage au filtre utilisé, en fonction de la région étudiée. Et toujours associer un filtre à un fenêtrage.
Pour avoir un meilleur contraste sur des régions où les densités µ sont voisines, on utilise un filtre mou (résolution en densité) et une largeur de fenêtre serrée (par exemple pour l’abdomen ou le médiastin).
Pour avoir une bonne vue des détails il faut utiliser un filtre dur (de résolution spatiale) et une largeur de fenêtre large (par exemple pour l’os pour différencier l’os dur et l’os spongieux, ou pour le parenchyme pulmonaire pour différencier l’air des bronches).
La qualité de l’image
La résolution en densité (détails)
Définition : il s’agit de la capacité de reconnaitre la plus petite différence de contraste entre 2 structures.
Pour augmenter la résolution en densité il faut baisser la taille de la matrice pour avoir des pixels plus grands, augmenter la taille du FOV de reconstruction, augmenter l’épaisseur de coupe de reconstruction, et utiliser un filtre de résolution en densité.
Pour augmenter le contraste on peut aussi baisser les kV, faire une injection d’iode ou resserrer la largeur de la fenêtre.
La résolution spatiale et la résolution en densité évoluent de manière inverse pour tous ces paramètres.
La résolution spatiale (contraste)
Définition : il s’agit de la capacité de distinguer 2 structures de petite taille (quel que soit le contraste) ; c’est la taille du plus petit détail visible.
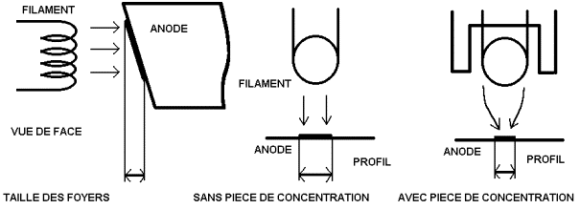
Elle dépend de la taille du foyer (flou géométrique), de la qualité de la collimation (flou de diffusion), et du nombre de photons qui stimulent les détecteurs (flou statistique).
Pour hausser la résolution spatiale il faut augmenter la taille de la matrice donc avoir des pixels de plus petite taille, baisser la taille du FOV de reconstruction, baisser l’épaisseur de coupe de reconstruction, et utiliser un filtre de résolution spatiale.
La résolution temporelle
Définition : il s’agit de la capacité de la machine à acquérir rapidement des données (<0.5s).
Plus la résolution temporelle est basse, plus le temps d’acquisition est faible, pour cela il faut que les détecteurs aient une faible rémanence.
Cette résolution est importante pour réduire le flou cinétique, mais également pour étudier les organes en mouvement (par ex : le cœur).
Le rapport signal sur bruit
Définitions :
- Le Signal (mA) est la partie informative de l’image.
Il dépend des paramètres d’acquisition (kV, mA, épaisseur de coupe, pitch, nombre de coupes).Plus l’irradiation est importante, plus il y aura de signal. On augmente les mAs pour avoir une meilleure signale.
- Le Bruit est le facteur de détérioration globale de l’image, de la chaine radiologique.
Il dépend du vieillissement du tube à rayons X, de la qualité des détecteurs, de la corpulence du patient, de la région à explorer, de l’épaisseur de coupes d’acquisition, de la matrice, des câbles etc. Moins il y aura d’irradiations, plus le bruit sera important. Le niveau de bruit d’une image reste en fait quasiment constant. Il faut plus d’épaisseur de coupe d’acquisition et augmenter la taille des pixels pour avoir plus de signal. S’il n’y a pas beaucoup de signal, les détails seront considérés comme du bruit.
Le rapport S/B caractérise donc la qualité de l’image.
Les paramètres d’acquisition
Les paramètres d’acquisition influencent la qualité de l’image, il faut savoir les adapter pour obtenir une image de bonne qualité.
Le FOV d’acquisition :
Il faut choisir un FOV d’acquisition au plus près de l’anatomie du patient s’il est trop grand ,le manipulateur sera obligé d’utiliser le zoom optique, et les pixels de la matrice seront trop gros et cela créera des marches d’escalier sur l’image. En appliquant un petit FOV d’acquisition, l’image aura une meilleure définition, on pourra voir mieux les limites des organes, calculer des distances ou faire des mesures de densité. 3 à 4 choix possibles de FOV d’acquisition, dépend du constructeur.
Le Pitch :
On privilégiera un pitch < 1 pour avoir une image de meilleure qualité. Les rayons traversent plusieurs fois une même région, l’épaisseur de coupe est irradiée plusieurs fois il y a donc une augmentation du nombre de mesures. Mais le temps d’acquisition est plus long et il y a une irradiation plus importante du patient (radioprotection).
L’épaisseur de coupes d’acquisition :
Le niveau de performance d’un scanner est lié au choix du nombre d’épaisseurs de coupes disponibles et à l’épaisseur de coupes la plus petite. Il faut que la plus petite épaisseur de coupes soit infra millimétrique > 0.5mm et la plus épaisse > 5mm. Dépend de ce qu’on veut voir à la base.
Les paramètres de reconstruction
Les filtres de reconstruction :
Il s’agit d’un calcul informatique de l’image native se faisant après l’acquisition des données, et ceci afin d’augmenter ou diminuer le contraste d’une image(le contraste permet de voir 2 structures de densités proches). « Durcir » l’image signifie diminuer le contraste et « Lisser » signifie augmenter le contraste. Les filtres vont de S : mou à E : dur. Donc pour un filtre mou on a un bon contraste un filtre standard un contraste correct et un filtre dur un mauvais contraste.
L’uniformité
Le filtre papillon et l’irradiation sur 360° permettent d’avoir une uniformité de l’image en tout point.
Pour mesurer l’uniformité de l’image, on utilise un ROI (Region Of interest), il s’agit d’une ellipse, d’une surface à l’intérieur de laquelle l’ordinateur fournit des critères de qualité de l’image, chiffrés en U.H. Il est placé après l’acquisition.
On teste le scanner avec un fantôme et on place plusieurs ROI pour mesurer si on a la même qualité image en tout point (même rapport S/B) = maintenance 1 fois par mois.
Pour la clinique le ROI a d’autres indications comme mesurer des lésions hépatiques etc, ou permet de lancer une injection au temps voulu.
II. Les artéfacts
Artéfacts métalliques (ou en « phare ») :
Origine : objet métallique dans le champ d’acquisition (boutons, fermeture éclair, bijoux, prothèse orthopédique …).
Effets sur l’image : hyperdensité centrale avec des traits hypodenses en périphérie.
Moyens de les atténuer : préparation physique du patient, enlever les vêtements les bijoux, augmenter les kV.
Artéfacts de mouvement
Origine : flou cinétique de respiration, battements cardiaques, mouvements du patient, de déglutition.
Effets sur l’image : dédoublements des bords de la structure qui bouge.
Moyens de les atténuer : préparation psychologique du patient, apnée, moyens de contention (sangle, coussins etc.), augmenter le pitch donc augmenter la vitesse de la table (acquisition hélicoïdale), augmenter l’incrément (en acquisition séquentielle), synchronisation cardiaque ou respiratoire.
Artéfacts de volume partiel
Origine : quand 2 tissus de densités très différentes se trouvent dans le même voxel, le processeur vectoriel calcule la moyenne des densités de deux structures (donc on obtient des niveaux de gris au lieu d’avoir du blanc et du noir = diminution du contraste) , donc les limites deviennent floues et la densitométrie fausse; ce qui peut causer un mauvais diagnostic en cas de placement de ROI ; le ROI mesure la densité moyenne d’un tissu à l’intérieur d’un cercle (moyenne de chaque densité des pixels).
Effets sur l’image :
Moyens de l’atténuer : baisser l’épaisseur de coupe (diminue l’épaisseur du voxel), augmenter la taille de la matrice (diminue la taille des pixels).
Artéfacts en « cible »
Origine : problème de calcul informatique de l’image par l’ordinateur dû aux détecteurs, cercles clairs concentriques sur l’image ou produit de contraste sur l’anneau du statif.
Effets sur l’image : si la cible est au milieu de l’image c’est dû aux détecteurs, si la cible est sur les côtés c’est dû aux produits de contraste.
Moyens de les atténuer : calibrer une fois par semaine le scanner, si le problème est non résolu changer un ou plusieurs détecteurs par le constructeur ; et nettoyer régulièrement le statif. Calibration : coupes de scanner dans le vide pour réinitialiser les détecteurs.
Artéfacts de durcissement de faisceau
Origine : lors de la traversée d’une structure dense à examiner, le faisceau de rayons x (polychromatique) subit une modification de son spectre avec élimination de la composante molle du faisceau.
Effet sur l’image : il y a apparition de traits d’hypodensité.
Moyens de les atténuer : augmenter les kV, filtre papillon.
Artéfacts de cone beam :
Origine : dû à la conicité du faisceau de rayons x et à l’augmentation de la taille du détecteur dans l’axe z ; le faisceau est perpendiculaire sur les barrettes centrales et oblique sur les barrettes externes, donc déformation de l’image aux extrémités
Effets sur l’image : les bords sont déformés dans le sens où il y a les détecteurs
Moyens de les atténuer : on ne peut rien faire
Artéfacts de moulin à vent
Origine : Artéfacts cinétique du au mouvement de la table. Lorsque la table bouge trop vite
Effets sur l’image : Image pixélisée
Moyens de les atténuer : Baisser la vitesse de la table (donc on baisse le Pitch)
Modes de traitement de l’image
A la base le scanner fait des reconstructions en axiale.
MPR (multi planar reconstruction) :
Il s’agit d’un mode de traitement de l’image facilement accessible sur la console du scanner. Cette reconstruction multi planaire 2D permet en effet de réaliser à travers le volume d’acquisition des coupes bidirectionnelles frontales, sagittales, obliques ou curvilignes. Il permet, notamment, de mettre dans un plan toute courbe arbitraire dans le patient. Pour obtenir des images analysables, en particulier pour éviter l’aspect en « marches d’escalier », il est souhaitable de réaliser à l’acquisition des coupes jointives ou chevauchées avec un pitch égal ou inférieur à 1 et de reconstruire en chevauchant les coupes.
(Curviligne : il s’agit de suivre une structure de trajet sinueux et de la reconstruire dans un seul plan, comme si elle était étalée à plat. Ce type de reconstruction est particulièrement important pour l’étude des vaisseaux)
Reconstruction 3D surfacique :
Il procure une vision tridimensionnelle extérieure d’éléments anatomiques et pathologiques. Il nécessite plusieurs traitements de l’image, dont le plus important est la détermination du seuillage des voxels. Ce seuillage permet de sélectionner certains éléments anatomiques ou pathologiques dont la densité correspond aux pixels choisis. Les surfaces sont créées en reliant tous les pixels correspondant à la même atténuation.
Selon l’échelle de pixels choisis, nous pouvons obtenir un moule positif ou négatif de l’objet étudié. Sur l’image ainsi obtenue, il est possible grâce à un bistouri électronique de se débarrasser des éléments anatomiques qui gênent la lecture. Il est possible également d’appliquer une lumière imaginaire, se reflétant sur les surfaces, leur permettant d’apparaître sous différents niveaux colorimétriques à on prend un fenêtrage correspondant à la couche anatomique à étudier, et les couches pas intéressantes sont supprimées.
Reconstruction 3D volumique :
Le rendu volumique attribue des opacités et des couleurs aux différents tissus en fonction de leur atténuation. De plus il est possible d’enlever certains organes en définissant une certaine fenêtre de seuils ou en les enlevant à l’aide d’un crayon électronique.
Des algorithmes de reconstructions complémentaires sont possibles telles que le Maximum Intensité Projection (MIP) qui sélectionne tous les pixels d’intensité maximale (bonne visibilité des vaisseaux injectés et des parois des bronches, et des os). Existe aussi le minimum Intensité Projection (minIP) qui sélectionne tous les pixels d’intensité minimum (bonne visibilité de l’air dans les bronches).
- Ex : Sang iodé : +150 Unité Hounsfield. Lors d’injection.
Endoscopie virtuelle
Coloscopie virtuelle, (acquisition procubitus, décubitus -> lorsque le colon est rempli d’air), mode ciné …
La radioprotection
Index de dose scanographique (IDS ou CTDI)
Le CTDI (sigle pour Computed Tomography Dose Index) est l’index de dose en scanographie correspondant à la dose par patient et par coupe. Cet index ne reflète pas la dose totale reçue par le patient. Elle s’exprime en mGy.
L’Indice de Scanographie Volumique (IDSv ou CTDI vol)
Est égal en mode hélicoïdal à l’Indice de dose de Scanographie pondéré IDPS ou CTDIw (weighted Computed Tomography Dose Index) divisé par le pitch.
Le Produit Dose Longueur (PDL) :
Il a été défini par analogie avec le produit dose surface utilisé en radiologie conventionnelle, et pour rendre compte de la dose délivrée au cours d’une procédure complète.
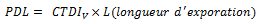
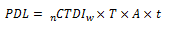
Où nCTDIw est le CTDI pondéré normalisé en mGy/mAs, T est l’épaisseur de coupe, et A x t représente la charge totale (mAs) de l’acquisition.
Plus simplement, le PDL est égal au produit du CTDIvol par la longueur explorée.
PDL= CTDI vol x L
L étant la longueur d’acquisition (programmée sur le topogramme)
Ce produit s’exprime logiquement en gray x cm. L’intérêt principal de cette grandeur est qu’elle représente exactement l’exposition en affectant la dose au volume exploré. Elle permet donc, en prenant en compte les organes figurant dans ce volume, de calculer ou d’estimer la dose efficace.
- Si on diminue T alors A et t vont augmenter pour avoir un bon rapport signal/bruit, du coup le PDL va augmenter. Donc plus l’épaisseur de coupe sera fine, plus la dose sera grande.
Pas de tablier plombé dans le champ d’acquisition, car sinon le scanner ou l’amplificateur va augmenter les constantes.
Paramètres réglés par le manipulateur :
- Tension : Passer de 120 à 140 kV augmente la dose d’environ 50 %.donc il faut diminuer les Kv attention à la résolution en densité et au rapport signal sur bruit.
- Charge : baisser les mAs mais baisse du signal donc baisse du rapport signal sur bruit.
- Epaisseur de coupes ou collimation dans l’axe tête pied : pour ne pas voir la pénombre la collimation est toujours plus grande que l’épaisseur de coupe choisie, donc il y a une hausse de la dose au patient alors que les photons X émis ne participent pas à la construction de l’image. Donc il faut bien choisir son épaisseur de coupe.
- Epaisseur de coupes à la reconstruction : pour reconstruire en infra millimétrique il faut avoir choisi une épaisseur de coupe à l’acquisition de l’ordre de 0.625 donc bien choisir son épaisseur de coupe à l’acquisition évite de recommencer l’acquisition. Attention au rapport signal sur bruit.
- Pitch voir chapitre précédent
Dispositifs de réduction de dose :
- Filtre papillon voir chapitre précédent à enlève les photons de basses énergies qui irradie trop le patient et qui ne servent pas à l’image.
- Collimateur de champ ou FOV adapter le champ à la taille de la structure à étudier.
Options logicielles :
Modulation en fonction de l’incidence sur chaque rotation (épaisseur du patient)
Les corps humains sont plus épais dans le plan frontal que dans le plan sagittal. L’émission des X sera donc programmée pour être plus importante à 90° et 270° qu’à 0° et 180°.
Modulation en fonction de la position en Z (axe tête pied)
Il s’agit d’adapter la charge en fonction de l’absorption de chaque « tranche » du volume, déterminée au préalable par les mesures d’absorption sur les topogrammes de face et de profil. Le crane est plus petit que le bassin par exemple.
Sur le scootview, le scanner va voir les pixels les plus dense et les moins dense et va en fonction de ça il va adapter la dose lors de l’acquisition. Hyperdense : augmenter les constantes. Hypodense : baisser les constantes.
Modulation en fonction de l’absorption mesurée en cours de rotation
Elle est plus sophistiquée que la simple modulation en fonction de l’incidence du tube, car elle mesure l’absorption du sujet, pour la coupe considérée, sur la première partie de la rotation et module la charge sur la deuxième partie, en fonction des données recueillies.
Les mesures d’absorption sont effectuées pendant la première moitié de la rotation. L’émission des X est ensuite modulée, pour la demi-rotation suivante, en fonction de l’absorption mesurée dans la position angulaire symétrique.
Conclusion :
- Réduire l’intensité mAs
- Réduire la tension kV
- Augmenter le pitch
- Limiter les acquisitions
L’avenir du scanner
L’avenir du scanner est d’augmenter la finesse du diagnostic tout en réduisant les doses au patient.
Le foyer Flottant :
L’anode serait mobile ce qui empêcherait sa chauffe car elle serait exposée à des endroits différents et le système n’accumulerait pas de chaleur pendant l’exposition.
De plus une même région anatomique est couverte 2 fois au même instant due à la double source d’irradiation.
Les détecteurs reçoivent une double information et reconstruisent informatiquement 32 coupes en 64 coupes deux fois plus fines.
La double énergie :
La double énergie se traduit par la possibilité d’obtenir une image à partir de 2 énergies différentes. Chacune des énergies met en avant des éléments anatomiques spécifiques visualisés à des énergies différentes.
Pour cela il y a 2 méthodes :
- Le Switch (kilovoltages différents pour un même tube) oblige les détecteurs à avoir une faible rémanence et une rapidité de réception des informations (construction rapide) mais il y a une bonne réduction de dose et une meilleure différenciation que la technique double tube.
- La méthode double tube est la plus techniquement réalisable, et obtient de meilleure résultats sur la soustraction des images (en post-traitement) et sur certaines pathologies (calcul de sténose carotidienne ….). La résolution temporelle est aussi meilleure, ce qui permet d’améliorer les scanners cardiaques et de faire des acquisitions 4D (la table a un mouvement bidirectionnelle couplé à un gating respiratoire).
Les détecteurs bicouche :
- Un pour la basse énergie
- Une pour la haute énergie
L’imagerie spectrale :
La double énergie va permettre l’introduction de l’imagerie de type spectrale au scanner avec tous les avantages diagnostiques : soustraire, additionner chaque élément tissulaire de l’image obtenue. Ainsi l’appareil spectral pourra séparer en différents spectres chaque élément formant l’image. Donc on pourra caractériser le tissu d’un organe.

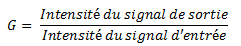
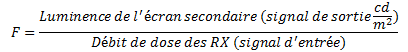




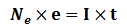
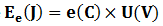
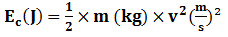
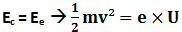
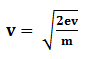
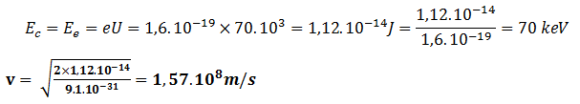
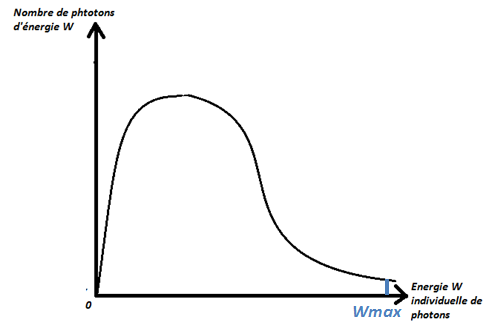
 Condition pour que le photon de fluorescence émis soit un photon X visible en radiodiagnostic
Condition pour que le photon de fluorescence émis soit un photon X visible en radiodiagnostic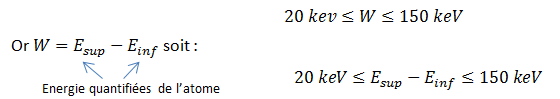
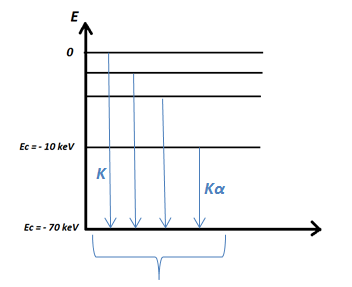 Spectre résultant
Spectre résultant