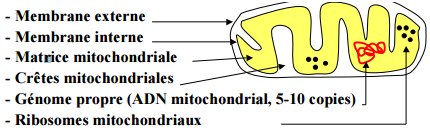
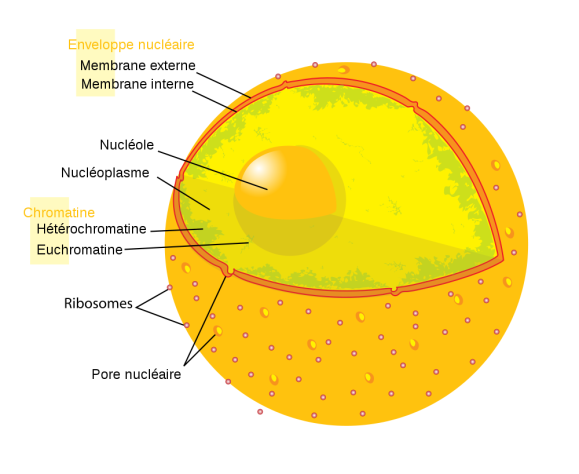
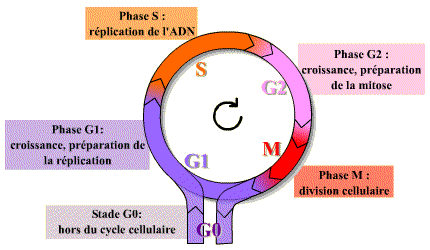
L’information génétique est contenue dans les chromosomes sous forme de gènes. Cette information génétique doit être :
- Conservée dans la descendance des cellules au cours de la division cellulaire
- Exprimée au sein des cellules de l’organisme pour permettre son développement et son fonctionnement
- Transmise dans la descendance d’un individu au cours de la reproduction
Conservation de l’information génétique
L’information génétique ne doit ni être modifiée, ni perdue lors de la division cellulaire afin de transmettre un patrimoine identique d’une cellule à l’autre.
L’information génétique est conservée entre générations de cellules grâce au mécanisme de réplication.
Expression de l’information génétique : la synthèse des protéines
Gène : plus petite fraction d’ADN capable de diriger la synthèse d’une protéine.
Génome : ensemble des gènes d’une espèce donnée regroupés en chromosomes.
Le génome humain comprend environ 30000 gènes. Dans le cytoplasme l’information génétique détenue par l’ADN est traduite sous forme de chaîne polypeptidique par un mécanisme biologique complexe appelé « traduction ».
Lien noyau-cytoplasme
La synthèse des protéines a lieu dans le cytoplasme alors que l’ADN des cellules en interphase se trouve dans le noyau. Il faut donc un messager et un décodeur capables d’assurer la synthèse des protéines à partir des informations détenues par l’ADN.
L’ARN messager ou ARNm : information nécessaire pour la synthèse d’une chaine polypeptidique. Environ 20% de l’ADN codent pour la synthèse d’un ARNm. Ce sont des acides nucléiques à vie courte.
L’ARN ribosomal ou ARNr : entre dans la constitution des ribosomes, acteurs de la traduction.
L’ARN de transfert ou ARNt : décodeur de l’information détenue par l’ARNm.
Remarque : l’ADN qui se trouve dans la région organisatrice du nucléole code pour la synthèse de l’ARNr. D’autres séquences d’ADN codent pour l’ARNt. L’ARNt et l’ARNr sont des produits finaux.
La synthèse des protéines se fait en deux temps :
- La transcription : processus permettant la synthèse d’un ARN à partir de l’information génétique.
- La traduction : déchiffrage du message conduisant à la synthèse d’une chaîne polypeptidique.
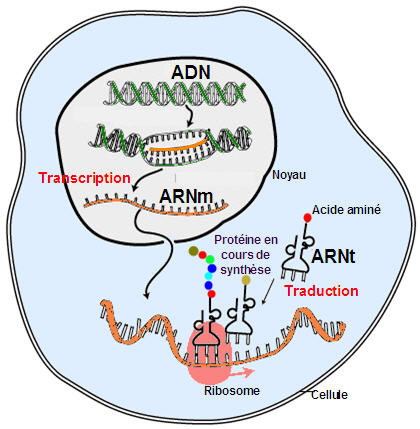
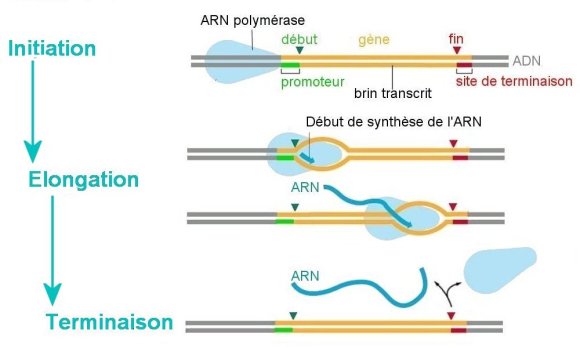
La transcription
Caractéristiques
Basée sur le principe de complémentarité des bases azotées. Elle nécessite de très nombreuses enzymes dont l’ARN polymérase ADN dépendante. Elle nécessite de l’énergie sous forme d’ATP. Elle se fait dans le sens 5’P à 3’OH à partir d’un brin matrice 3’OH à 5’P, comme la transcription est antiparallèle, le brin d’ADN sera orientée en 5’P vers 3’OH.
Un seul brin de double hélice sert de matrice à la synthèse de la molécule d’ARN : celui orienté dans le sens 3’OH vers 5’P.
Déroulement
S’effectue en trois étapes :
- Initiation
- Elongation
- Terminaison
L’ARN polymérase catalyse la formation de la liaison 3’-5’ phosphodiester entre les ribonucléotides. La croissance de la chaine se fait dans le sens 5’P à 3’OH. La transcription s’arrête quand l’ARN polymérase rencontre une séquence particulière appelée « séquence de terminaison ». Un ARN pré-messager se détache de la matrice d’ADN.
Caractéristiques de la chaine d’ARN pré-messager synthétisée :
- Complémentaire
- Antiparallèle de la chaine d’ADN matrice
Traitement de l’ARN pré-messager
L’ADN contient des régions codantes ou exons et des régions non codantes ou introns. L’ARN pré-messager résulte de la transcription complète du brin d’ADN. Des complexes enzymatiques d’épissage sont chargés d’enlever les introns et de lier ensemble des exons : obtention d’un ARNm mature. Il se lie alors à des protéines qui vérifient son intégrité etl e guident vers les pores nucléaires.
La traduction
Code génétique
L’information génétique nécessaire à la synthèse des protéines est exprimée au niveau de la molécule d’ARN en nucléotides à l’aide de quatre bases azotées. Les protéines sont synthétisées à partir d’acides aminés. Il existe donc un système de correspondance, une sorte de « dictionnaire », qui fait correspondre à un triplet de nucléotides ou codon, un acide aminé.
Ce système de correspondance est appelé « code génétique ».
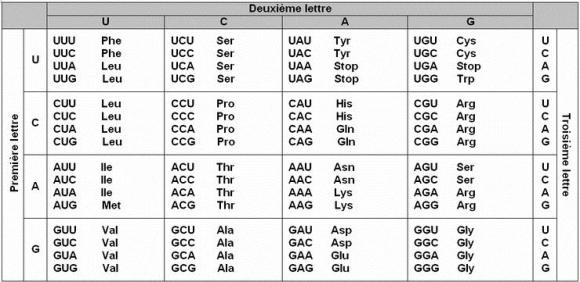
Remarques : il existe 64 codons alors qu’il n’y a que 20 acides aminés qui entrent dans la constitution des protéines. Il existe :
- Trois codons stop: signaux d’arrêt de la traduction
- Des redondances, un même acide aminé peut correspondre à des codons différents. C’est une forme de protection contre les erreurs de transcription ou de traduction.
Outils de la traduction
La traduction correspond au déchiffrage de l’information porté par l’ADN conduisant à la synthèse d’une chaine polypeptidique. Elle nécessite :
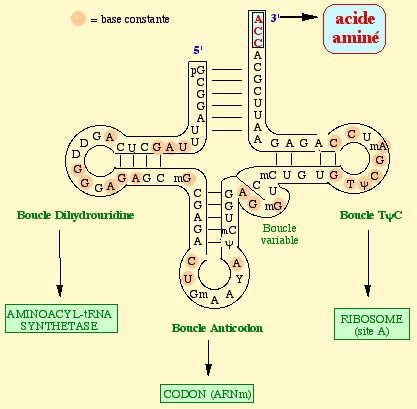
Des ARNt : molécules adaptatives servant d’intermédiaires entre l’ARNm et les acides aminées et possédant deux régions :
- Une région de reconnaissance de l’ARNm, appelée anticodon: la reconnaissance se faisant selon le principe de complémentarité des bases azotées.
- Une région qui se lie avec spécifiquement avec un acide aminée correspondant au codon de l’ARNm.
Des ribosomes assurant :
- La reconnaissance entre le codon de l’ARNm et l’anticodon de l’ARNt.
- La formation de la liaison peptidique entre les acides aminés grâce à une enzyme, la peptidyl-tranférase.
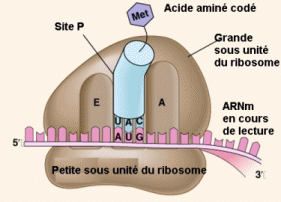
Les ribosomes possèdent 3 sites de liaison :
- Un site A (aminoacyl) pour la fixation de l’ARNt porteur d’un acide aminé arrivant (aminocyl – ARNt)
- Un site P (peptidyl) pour l’ARNt porteur de la chaine peptidique en croissance
- Un site E (exit) pour l’ARNt sortant
Déroulement
La traduction se déroule en 3 étapes :
- Initiation
- Elongation
- Terminaison
La traduction débute par :
- La mise en place sur le site P de la petite sous unité du ribosome de l’ARNt d’initiation porteur de la méthionine
- La mise en place de la petite sous unité du ribosome au niveau du codon initiateur de l’ARNm : codon …
- L’établissement d’une liaison codon initiateur (ARNm) – anticodon (ARNt d’initiation)
- L’arrivée de la grande sous unité ribosomale : ribosome fonctionnel: nécessite des enzymes et de l’énergie
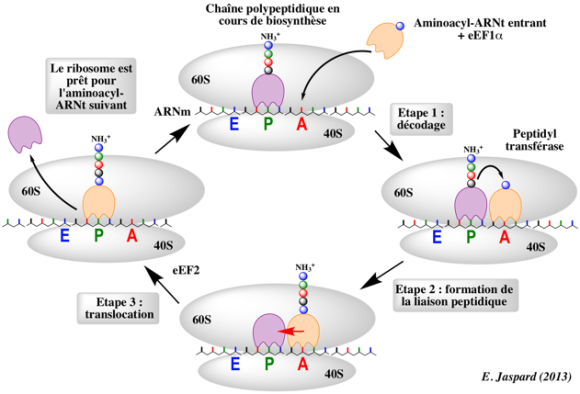
La traduction se poursuit par :
- La fixation de l’aminocyl ARN t n°2 sur le site A du ribosome
- La formation de la liaison peptidique entre les deux premiers acides aminés (réaction catalysée par la peptidyl-transférase)
- La rupture entre l’ARNt d’initiation et son acide aminé
- La translocation du ribosome : déplacement du ribosome sur l’ARNm
- L’ARNt d’initiation se retrouve sur le site E puis dans cytosol
- L’ARNt porteur de l’acide aminé n°2 lié à méthionine se trouve sur le site P
- L’arrivée de l’aminocyl ARNt n°3 sur le site A du ribosome
La terminaison apparait lorsque le ribosome rencontre : un codon STOP
- La chaine polypeptidique se détache du ribosome
- Les deux sous unités du ribosome se séparent
- La chaine polypeptidique acquiert sa structure tridimensionnelle
Remarques :
Lors de la synthèse protéique, le premier acide aminé incorporé est à l’extrémité N-terminale de la chaine polypeptidique. La méthionine peut être enlevée après la synthèse.
Vitesse du processus de traduction : 15 acides aminés mis en place par seconde. Au fur et à mesure que le ribosome avant sur l’ARNm et que le début de la chaine se libère, un autre ribosome peut s’y fixer et ainsi de suite…
Un ARNm est « lu » par plusieurs ribosomes en même temps : polysome.
Mutation de l’ADN – conséquences sur les protéines
Il peut arriver que, lors de la réplication de l’ADN, malgré les systèmes de correction, l’ADN polymérase commette des erreurs d’appariement ce qui provoque l’apparition de mutations.
Définitions et caractéristiques
Modification localisée du matériel génétique, elle peut être ponctuelle (1 seul acide aminé concerné) ou porter des régions plus ou moins longues d’ADN.
Les conséquences sur la protéine dépendant de la nature de la mutation. Ces mutations peuvent être classées en deux grands types :
Mutations entraînant un décalage du cadre de lecture
- Insertion d’un nucléotide
- Délétion d’un nucléotide
Dans les deux cas, la séquence en acides aminés de la protéine en aval de la mutation est totalement modifiée.
Conséquences : modification de la fonction de la protéine. Si délétion : peut-être tronquée.
Mutations n’entraînant par un décalage du cadre de lecture
- Substitution un codon :
Cas 1 : mutation faux sens : la séquence protéique est modifiée au niveau d’un seul acide aminé. Selon la nature de l’acide aminé, la fonction de la protéine est plus ou moins modifiée.
Cas 2 : mutation silencieuse : la séquence est modifiée. N’engendre pas de modification dans la fonction et la configuration de la protéine. La mutation est dite neutre si elle engendre le remplacement d’un acide aminé par un autre sans modification du fonctionnement de la protéine.
Cas 3 : mutation non-sens : au lieu d’avoir la séquence normale on arrive à un CODON STOP. La protéine est raccourcie et peut être non fonctionnelle.
BILAN :
Elles peuvent induire des maladies pathogènes. Elles peuvent être plus ou moins étendues, d’un simple changement de nucléotides à toute une portion d’ADN. Elles ne sont transmises aux descendants que si elles affectent les cellules germinales.
Les mutations spontanées sont rares. Elles peuvent être liées à des facteurs externes. Il existe des agents chimiques (certains produits chimiques) ou physiques (rayons X, rayonnement UV) qui interagissent avec l’ADN et induisent différents types de modifications (transformations des bases azotées, modifications de la séquence des nucléotides, cassures) : ce sont des agents mutagènes.
Transmission de l’information génétique
Caryotype
L’information génétique est contenue dans les chromosomes. Le caryotype permet de visualiser les chromosomes sous leur forme la plus condensée.
Un caryotype présente de manière organisée les chromosomes d’une cellule observée en microscopie optique. Ils sont rangés par paire de chromosomes homologues selon la taille et la disposition du centromère.
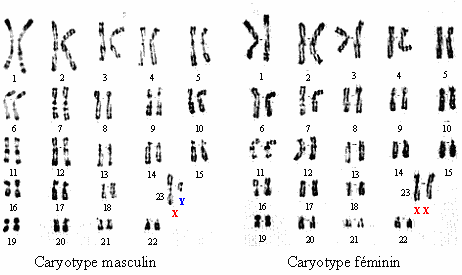
Les noyaux des cellules humaines à l’exception des gamètes renferment 46 chromosomes, nombre diploïde soit 23 paires de chromosomes homologues. Dans chacun d’eux, un est d’origine paternelle et l’autre maternelle. Une de ces paires est constituée des chromosomes sexuelles, les 44 autres chromosomes, forment les 22 paires d’autosomes.
Chez une femme : 44 chromosomes + XX
Chez un homme : 44 chromosomes + XY
La méiose
La formation des gamètes (gamétogenèse) chez l’homme et la femme fait intervenir la méiose. Elle comprend deux divisions nucléaires successives qui produisent quatre cellules fines. Suite à :
La première division : 2 cellules avec n chromosomes (haploïde) à 2 chromatides chacun : division réductionnelle
La deuxième division : 4 cellules avec n chromosomes à 1 chromatide chacun : division équationnelle.
Fonctions fondamentales de la méiose :
- Réduit le nombre de chromosomes par deux, les cellules obtenues sont donc haploïdes et possèdent donc 23 chromosomes.
- Brassage génétique
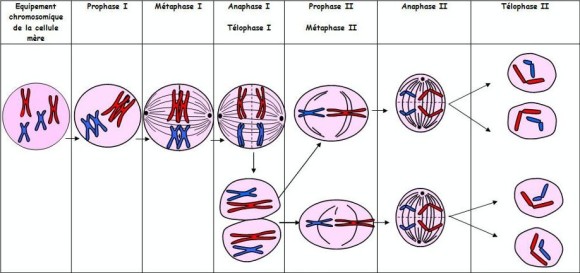
Méiose I
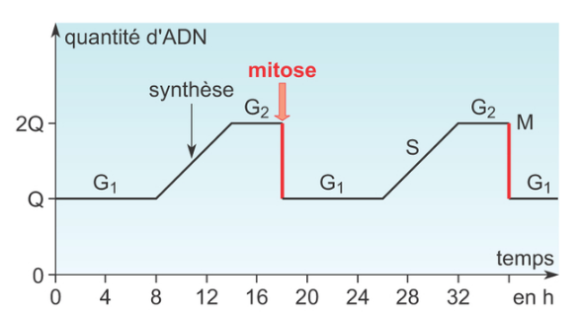
Prophase I : comme dans la mitose, la réplication de l’ADN a lieu avant le début de la méiose. Au cours de la prophase :
- Condensation des chromosomes
- Disparition de l’enveloppe nucléaire et le nucléole se désorganise
- Formation du fuseau mitotique
Mais cette étape est marquée par la synapsis : les chromosomes homologues s’accolent sur leur longueur pour former des tétrades. Cette étape est marquée par le croisement à plusieurs endroits des chromatides de chaque paire de chromosomes homologues (chiasmas). Des fragments de chromosomes sont échangés entre les chromosomes homologues. Intérêt : permet l’échange de matériel génétique entre les chromosomes appariés.
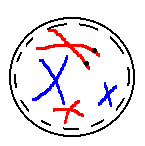
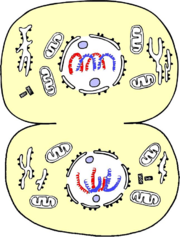
Métaphase I : les chromosomes de chaque paire de chromosomes homologues se placent de part et d’autre du plan équatorial.
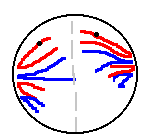
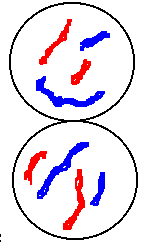
Anaphase I : contrairement à ce qui se passe lors de la mitose, les centromères ne se divisent pas lors de l’anaphase I lors de la méiose I. Ce sont les chromosomes homologues qui se séparent l’un de l’autre et qui migrent vers chaque pole de la cellule. Chacune des 23 paires de chromosomes est ainsi séparée.
Télophase I : les deux lots de chromosomes se décondensent. Une nouvelle enveloppe nucléaire se forme. Le fuseau mitotique se disloque. Chaque cellule fille possède un nombre haploïde de chromosomes (n chromosome à deux chromatides) : cette première division est dite réductionnelle.
Les cellules filles entrent en intercinèse avant le début de la méiose II.
Méiose II
La méiose II concerne les deux filles à n chromosomes issues de la méiose I. elle comprend une division nucléaire semblable à celle de la mitose qu’on appelle la division équationnelle.
A l’issue de la méiose II, nous avons 4 cellules à n chromosomes de 1 chromatide chacun.
Vocabulaire génétique
Locus : zone de localisation d’un gène sur un chromosome. Chaque paire de chromosomes homologues d’une cellule est constituée d’un chromosome d’origine paternelle. Les chromosomes étant appariés, on peut donc rencontrer deux versions d’un même gène, l’une d’origine maternelle, l’autre paternelle.
Allèle : version d’un même gène situé sur le chromosome d’origine maternelle et le chromosome d’origine paternelle. Les deux allèles d’un même gène occupent le même locus. Dans une population, un gène peut exister sous plusieurs formes, le locus et la fonction restant constants.
Individu « homozygote » : possède deux allèles de séquence nucléotidique identique pour un gène donné.
Individu « hétérozygote » : possède deux allèles de séquence nucléotidique différente pour un gène donné.
Allèle dominant : allèle qui s’exprime (P)
Allèle récessif : allèle qui reste « muet » (p). Un allèle récessif ne s’exprime qu’à l’état d’homozygote.
Allèles codominants : les deux allèles s’expriment en même temps.
Allèle létal : forme mutante d’un gène, létale à l’état d’homozygote.
Gène polyallélique : représenté par plus de deux allèles.
Génotype : patrimoine génétique d’un individu.
Phénotype : ensemble des caractères d’un individu.
Hérédité liée au sexe ou gonosomale : gène étudié porté par un chromosome sexuel.
Hérédité autosomale : gène étudié porté par un chromosome autosome.
Sources sexuelles des variations génétiques
Chaque individu (à l’exception des vrais jumeaux) est différent avec un génotype différent et phénotype unique dû :
- Au brassage interchromosomique (crossing over – enjambement)
- Au brassage intrachromosomique
- A la fécondation
La ségrégation indépendante des chromosomes
Au cours de la méiose I, lors de la gamétogenèse, les paires de chromosomes homologues s’accolent pour former des tétrades. L’alignement et l’orientation des tétrades sur le fuseau mitotique lors de la métaphase I se fait au hasard : les chromosomes d’origine maternelle et paternelle sont distribués au hasard, ce qui conduit à un brassage interchromosomique.
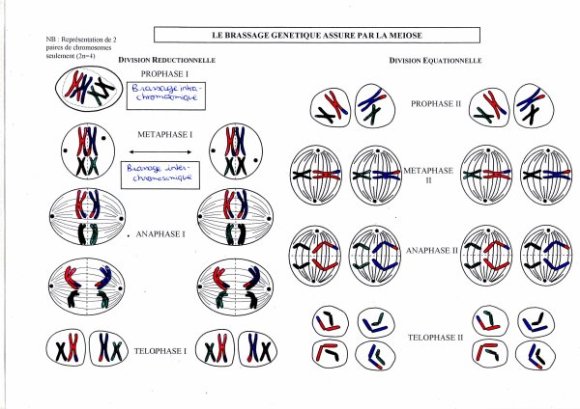
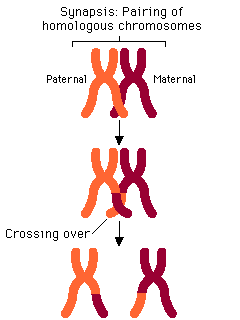
Enjambement des chromosomes ou crossing-over
Intérêt : certains gènes du chromosome d’origine paternelle se retrouvent sur le chromosome maternelle et inversement. C’est le brassage intrachromosomique et donne des chromosomes recombinants.
Transmission des gènes
Hérédité autosomique dominante et maladies associés
Concerne les caractères héréditaires portés par les autosomes et gouvernés par les allèles dominants. Caractéristiques :
- Caractère dominant lorsqu’il s’exprime à l’état hétérozygote, quand un individu qu’un seul allèle dominant transmis par ses parents.
- Caractère héréditaire autosomique : se transmet aux descendants indépendamment du sexe.
Les maladies autosomiques dominantes sont portées par des allèles dominants sur les autosomes. Le génotype homozygote est beaucoup plus sévère voire létal.
Exemples de maladies autosomiques dominantes :
- Maladie osseuse (achondroplasie)
- Maladie du tissu conjonctif (maladie de Marfan)
- Déficits sensoriels (surdités, maladies ophtalmiques)
- Maladie générative (maladie de Huntington)
Hérédité autosomique récessive et maladies associées
Concerne les caractéristiques héréditaires portés par les autosomes et gouvernés par les allèles récessifs. Caractéristiques :
- Récessif lorsqu’il s’exprime que à l’état d’homozygote.
- Autosomique récessif se transmet indépendant
Exemples de maladies autosomiques récessives :
- La mucovisidose
- Des maladies de l’hémoglobine (drépanocytose)
- Des surdités
- Des cécités
- Des maladies métaboliques
Hérédité liée au sexe et maladies associées
Les chromosomes sexuels portent les gènes de nombreux caractères totalement indépendants du sexe. Chez l’homme, l’expression « lié aux sexe » désigne habituellement des caractères portés par les chromosomes X. Le père transmet les allèles au chromosome X à ses filles mais pas à ses fils puisqu’il leur transmet son chromosome Y. La mère peut transmettre les allèles liés au chromosome X, aussi bien à ses filles qu’à ses fils.
De nombreux caractères héréditaires portés par le chromosome X ne sont pas portés par le chromosome Y. Chez une femme, le caractère lié au sexe est donc porté par les deux chromosomes X et chez l’homme par un seul chromosome X.
Un tel caractère peut être dominant ou récessif et s’exprimer chez les femmes à l’état homozygote ou hétérozygote. Néanmoins, chez l’homme, le caractère s’exprime automatiquement quelle que soit la dominance : on parle de caractère hémizygote.
Exemples de maladies :
- L’hémophilie
- Le daltonisme
- La myopathie de Duchene
- Le syndrome de l’X fragile
Lorsque le caractère est situé sur le chromosome Y, il ne peut se transmettre que de père en fils.
Exemples de maladie :
- L’hypertrichose des oreilles


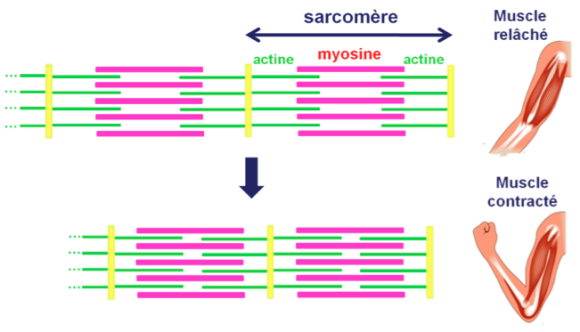
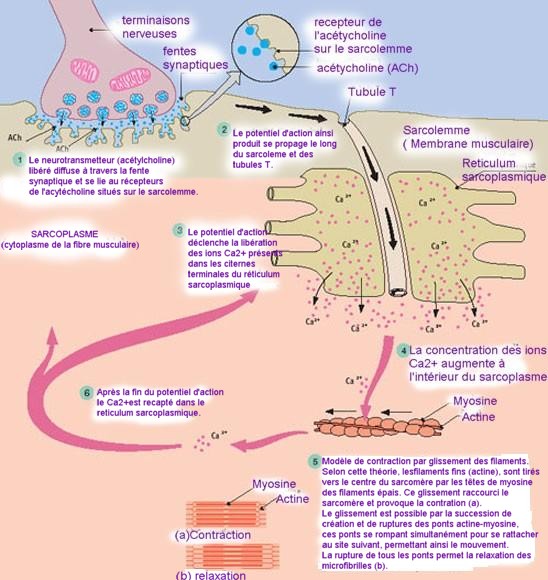
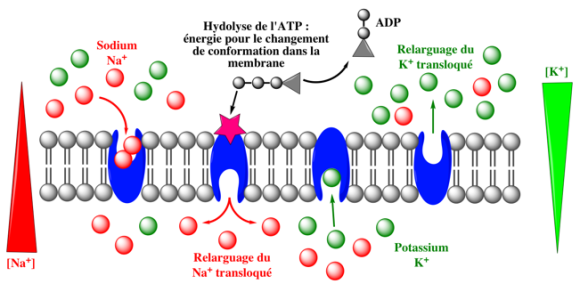 Potentiel gradué – Potentiel d’action
Potentiel gradué – Potentiel d’action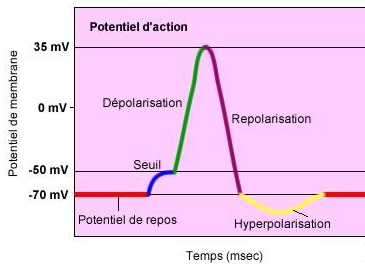
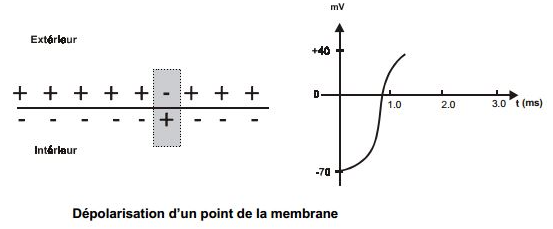
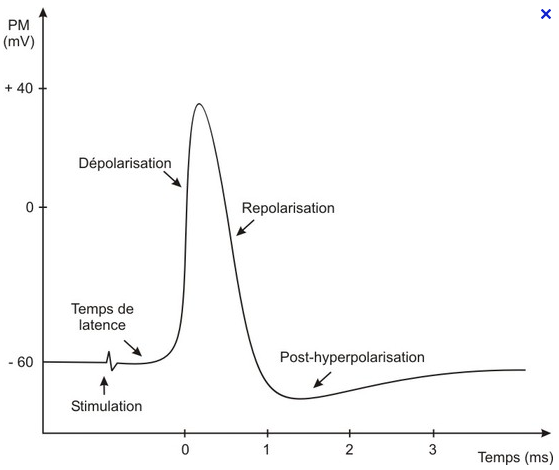
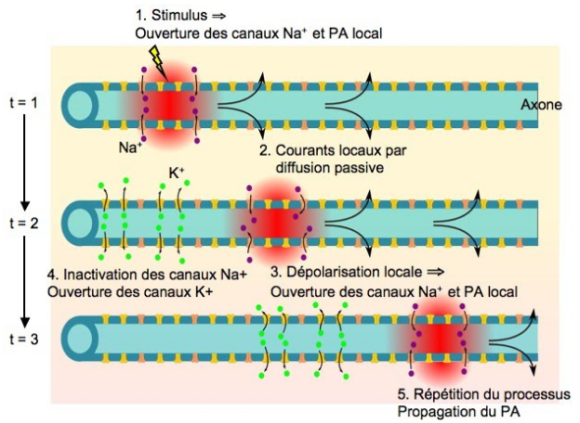 Vitesse de propagation
Vitesse de propagation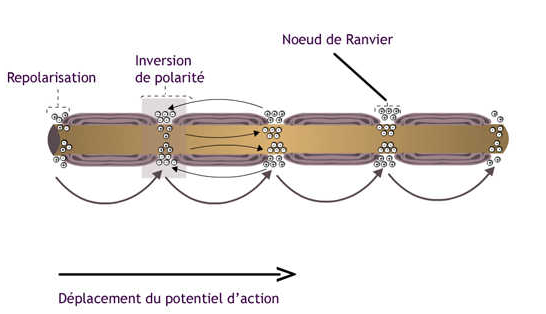


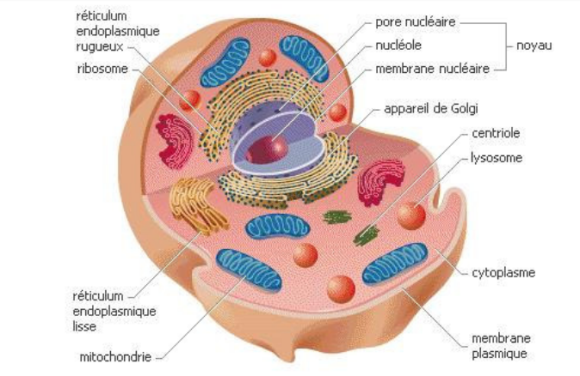 La membrane plasmique
La membrane plasmique